外科修复的传统挑战与Tissium的创新范式
长期以来,外科医生在组织修复领域面临着诸多挑战。传统的机械性修复手段,如缝合线和吻合钉,尽管应用广泛,却往往伴随着自身的局限性。这些方法可能对脆弱的组织造成二次损伤,导致术后疼痛、炎症,甚至影响组织的自然愈合过程。此外,现有的网片和医用胶水在生物相容性、粘合强度以及与湿润组织结合的能力方面表现不一,有时还会引发身体排斥反应,导致修复失败或并发症。这种对机械固定的高度依赖,限制了外科手术在微创和精确修复方面的进一步发展,也使得患者的术后恢复周期较长,功能性康复效果难以完全保证。
面对这些长期存在的痛点,麻省理工学院(MIT)衍生公司Tissium提出了一种革命性的解决方案:基于生物聚合物的组织修复平台。这项创新技术的核心在于其灵活、生物相容的聚合物材料,它能够与周围组织完美贴合,并在特定蓝光的激活下,实现对撕裂组织的牢固、无创粘合。这项技术的出现,旨在颠覆外科修复的传统模式,为医生提供一种更为温和、高效且能够促进患者更好康复的选择。
核心技术解析:生物聚合物的独特优势与光固化机制
Tissium生物聚合物平台的独特之处在于其精妙的材料科学设计。该平台的核心是一种专有的生物聚合物,其物理和化学特性经过精心调校,以适应人体复杂的生理环境。这种聚合物的特点在于其卓越的生物相容性,确保在植入体内后不会引发显著的免疫排斥反应或毒副作用。更重要的是,该聚合物的厚度和疏水性经过精确优化,使其能够在湿润的生物组织表面实现优异的粘附能力。这解决了传统粘合剂在潮湿环境下附着力不足的难题,为外科医生在复杂的体腔手术中提供了可靠的支持。
聚合物的激活过程是其创新性的又一体现。通过使用特定波长的蓝光照射,聚合物可在数秒内迅速发生光固化反应,从液体或凝胶状态转变为稳定的固态结构。这一过程不仅精确可控,而且是非热性的,避免了对敏感组织造成热损伤。固化后的聚合物能够紧密地包裹并连接受损组织,形成一个柔韧、坚固且与周围组织协调运动的修复结构。这种非侵入性的连接方式,与需要穿刺组织才能生效的缝合线和吻合钉形成鲜明对比,极大地降低了术后创伤和并发症的风险。
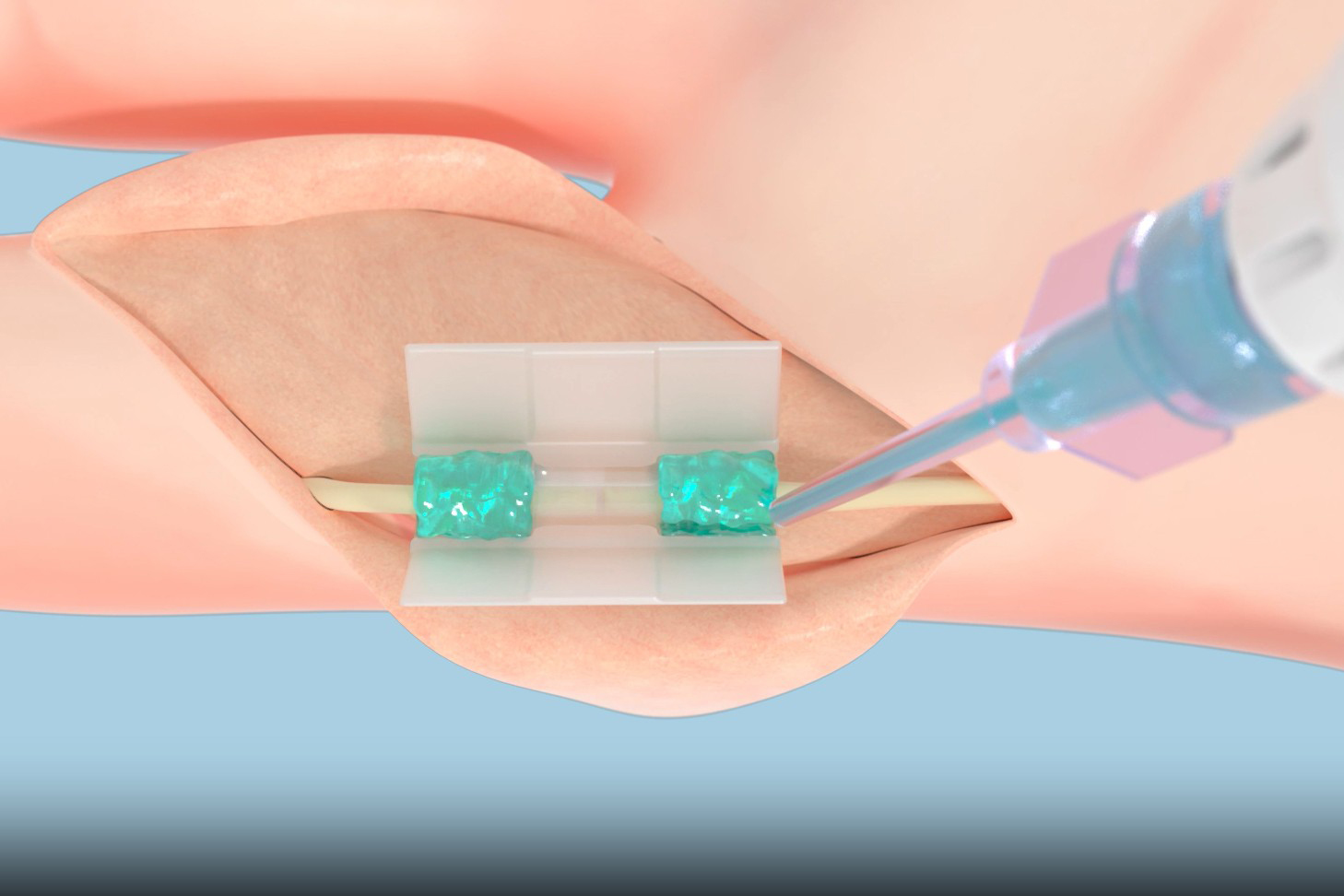
除了聚合物本身,Tissium的平台还包括一个3D打印的支架或腔室,用于引导和辅助聚合物的精确应用,特别是在神经修复等精细操作中。这种集成式的解决方案,不仅提升了操作的便捷性,也确保了修复的精准度和稳定性。该技术的出现,标志着外科修复从机械固定向生物粘合的范式转变,为实现微创、精准和快速康复的外科目标提供了坚实的基础。
FDA里程碑:神经修复领域的突破性进展及其深远影响
2025年6月,Tissium生物聚合物平台取得了公司发展史上一个重要的里程碑:其非创伤性、无缝合的周围神经修复解决方案获得了美国食品药品监督管理局(FDA)的De Novo营销授权。这一授权意义重大,它不仅是对Tissium技术新颖性和独特性的官方认可,更是为其首款产品的商业化铺平了道路。De Novo分类适用于那些现有市场上没有类似产品的创新型医疗器械,这进一步凸显了Tissium技术在医疗领域的开创性地位。
FDA的批准是基于严格的临床研究数据。一项针对12名周围神经损伤患者的临床试验显示出令人鼓舞的结果:所有完成随访的患者在术后12个月均恢复了受伤手指或脚趾的完全屈伸功能,并且没有报告任何疼痛。这项数据与当前缝合修复方法的低效形成鲜明对比——最近的一项荟萃分析显示,通过缝合进行神经修复的患者中,只有54%能够实现有意义的功能恢复。Tissium的柔性聚合物技术通过避免缝合带来的创伤、张力及错位问题,显著改善了患者的预后,提升了生活质量。
Maria Pereira,Tissium的联合创始人之一,强调了传统缝合技术在结果上的不确定性以及可能导致的创伤。她指出,缝合可能造成组织损伤、张力过大和对齐不良,这些因素都会影响患者的感觉、运动功能以及整体生活质量。Tissium的解决方案通过提供一种无创伤的方式来重新连接神经,有效避免了这些弊端。此次FDA的批准不仅是对Tissium多年研发努力的肯定,也为更广泛的无缝合组织修复应用奠定了监管基础,预示着该技术将在其他外科领域发挥巨大潜力。
从实验室到临床:Tissium的研发与转化之路
Tissium的诞生,源于麻省理工学院和哈佛大学的顶尖科研力量。早在多年前,作为MIT Institute Professor Robert Langer实验室的博士后研究员,Jeff Karp就致力于开发可生物降解、光固化的弹性材料,以应用于多种临床场景。2008年,Maria Pereira作为MIT葡萄牙项目(MIT Portugal Program)的访问博士生加入Karp实验室,专注于优化聚合物的厚度和疏水性,以提升其在湿润组织上的粘附性能。
正是Pereira将这一聚合物平台成功转化为了一个具有广泛医学应用潜力的固定平台。他们最初的灵感之一来源于波士顿儿童医院心脏外科医生Pedro del Nido提出的一个重大问题——新生儿先天性心脏病中的心脏穿孔缺乏合适的修复方案。Pereira及其团队随后在动物模型(大鼠和猪)上成功验证了该生物聚合物在不引起出血或并发症的情况下密封心脏穿孔的能力。这些早期的突破性研究奠定了Tissium商业化的基础。
2012年,制药行业资深人士Christophe Bancel在一次访问剑桥期间,与Karp、Pereira和Langer会面,首次接触到这项技术。在接下来的几个月里,Bancel与约15位来自不同领域的外科医生进行了深入交流,了解他们在手术中面临的挑战。这次广泛的调研使他坚信,如果这项技术能够成功应用于临床,将能解决外科领域一大系列难题,并获得医生们的极大热情和认可。在MIT技术许可办公室的协助下,Bancel将这项源自Karp在Langer实验室原创工作的聚合物技术从实验室推向了市场,并于2013年与Pereira、Karp、Langer等人共同正式创立了Tissium公司。

公司成立后,Tissium面临的挑战是将实验室技术转化为可商业化量产的产品。他们与专业的聚合物合成公司合作,并开发了一种创新的3D打印方法来生产用于包裹神经的聚合物外壳。Bancel指出,产品并非仅仅是聚合物本身,而是聚合物与配套附件的组合,关键在于外科医生如何使用它。因此,设计适合特定手术的附件变得至关重要。这一从基础研究到临床应用的转化过程,不仅展现了科学家的远见和毅力,也体现了产学研结合在推动医疗创新方面的巨大潜力。
多领域应用潜力:可编程平台的广阔前景
Tissium生物聚合物平台的独特之处在于其高度的“可编程性”。这意味着研究人员可以根据不同的临床需求,精确调整聚合物的降解速度和机械性能。例如,在需要临时支撑的应用中,可以选择快速降解的聚合物;而在需要长期稳定的结构修复时,则可选择降解缓慢或具有更高机械强度的材料。这种灵活性使得Tissium的技术能够适用于从神经到心血管系统,再到腹壁等各种组织类型和解剖部位。
目前,Tissium旗下有六款产品处于研发阶段,其中一项疝气修复的临床试验正在进行中,另一项心血管应用也即将启动。公司高层坚信,如果这项技术在一个应用领域取得成功,那么它很有可能在其他众多领域同样发挥作用。这种早期判断正在逐步得到验证,例如,尽管首次FDA批准针对神经修复,但该聚合物在封堵新生儿心脏缺损方面的早期研究已经显示出巨大潜力,这证明了其在不同组织类型上的适应性。
此外,公司对3D打印生产工艺的掌握,进一步拓宽了其应用边界。Karp解释说,3D打印技术不仅有助于广泛应用于医疗领域的组织固定,更重要的是,它使得从相同的聚合物平台制造各种可植入式医疗设备成为可能。这种结合了材料可编程性和制造灵活性的方法,为开发具有全新功能和能力的医疗器械打开了大门,例如个性化定制的植入物,或者能够随身体自然愈合过程而逐步降解和重塑的生物支架。这种多维度、可扩展的创新模式,预示着Tissium的平台有望成为未来医疗设备领域的重要基石。
展望未来:智能材料与医疗设备的深度融合
Tissium生物聚合物技术的成功,不仅仅是单一产品的胜利,更是智能材料科学在医疗健康领域深度融合的缩影。它挑战了外科修复长期以来依赖机械方法的传统观念,开辟了“无缝合”外科的新方向。通过最大程度地减少手术创伤、优化愈合环境并加速患者康复,这项技术有望显著提升全球患者的生活质量。
公司正积极鼓励医疗领域的专业人士与他们联系,共同探索该平台改善现有护理标准的新可能。这种开放合作的态度,与MIT始终秉持的创新和转化精神一脉相承。正如Jeff Karp和Robert Langer所言,能够将实验室的研究成果转化为真正改变患者生命的治疗方案,是每一个科研工作者的“梦想”。Tissium的FDA批准,正是这一梦想变为现实的有力证明,也预示着在生物医学工程和材料科学的交叉领域,未来将涌现出更多颠覆性的医疗突破。随着可编程材料和先进制造技术(如3D打印)的不断进步,我们有理由相信,智能、自适应的医疗设备将越来越多地走进临床,为人类健康带来前所未有的福祉。